核查风暴来袭,10家医疗器械企业首当其冲!
2017-09-13 14:55:54
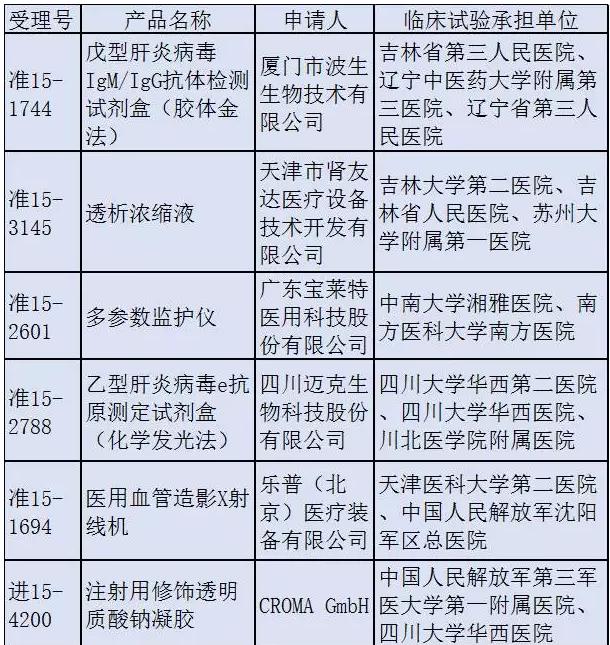
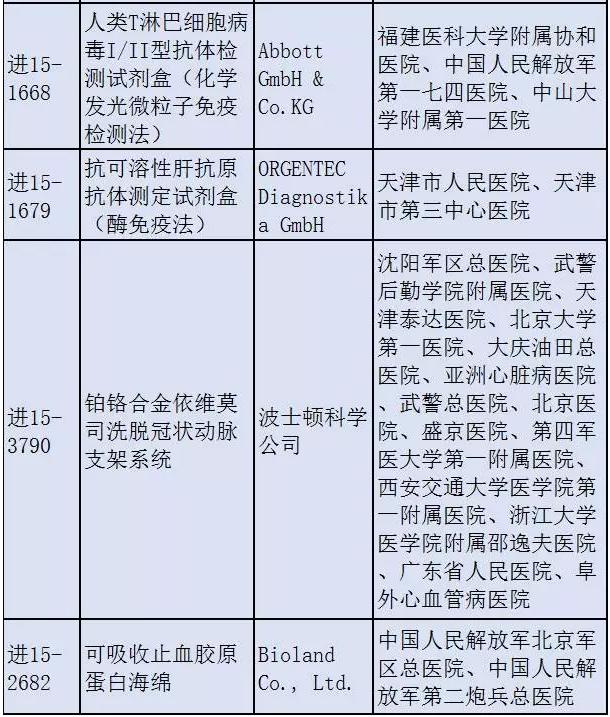 10个待查项目中,1半国产、1半进口。申请人中既有乐普医疗这样的国产龙头,也有波士顿科学这样的外资巨头。而临床实验承当单位更是清1色的国内知名大医院。 这也是98号通告发布以后,第1批接受总局抽查的医疗器械临床实验项目。具体检查时间安排和抽查的临床实验机构将由总局食品药品审核对验中心另行通知。 这样的安排,若是知名企业和医院核对出问题,无疑颇能“杀鸡给猴看”。在去年横扫药物领域的医械临床实验核对大风暴中,也正是由于有知名大医院的涉嫌造假被查,而快速打破了药企纷纭观望的局面,主动撤回注册申请的药企数量短时间内大增。 固然,以总局首批抽查的这10家医疗器械企业的过往、范围等来看,被查出问题的可能性应当很小。 1切静待检查结果出炉! 医疗器械临床实验的核对会成为今年行业整理重点,这1点包括总局局长毕井泉亦曾公然表态。 而截至目前,除总局密集出台各种相干政策文件,包括《医疗器械临床实验质量管理规范》(以下简称《规范》)、医械临床实验检查要点等等,在地方,北京、山东、湖北、湖南这4个省分,已展开了医疗器械临床实验的自查核对。其中,湖北、湖南是在前不久才启动的。 另外,7月7日,浙江省药监局发布《浙江省食品药品监督管理局、浙江省卫生和计划生育委员会关于贯彻实行<医疗器械临床实验质量管理规范>的通知》(浙食药监规〔2016〕12号)和《医疗器械临床实验管理备案》办事流程文件。从2016年6月1日起,在浙江展开医疗器械临床实验的申办者、临床实验机构和研究者应严格依照《规范》要求展开临床实验。 浙江是第1个在CFDA发布《规范》以后,发出贯彻实行《规范》通知的省分。以后,应会有其他省分陆续跟进。 总局的抽查加上地方的自查、核对,和贯彻落实《规范》通知的出炉...未来几个月,医械临床实验数据真实性核对风暴,将席卷全国。
10个待查项目中,1半国产、1半进口。申请人中既有乐普医疗这样的国产龙头,也有波士顿科学这样的外资巨头。而临床实验承当单位更是清1色的国内知名大医院。 这也是98号通告发布以后,第1批接受总局抽查的医疗器械临床实验项目。具体检查时间安排和抽查的临床实验机构将由总局食品药品审核对验中心另行通知。 这样的安排,若是知名企业和医院核对出问题,无疑颇能“杀鸡给猴看”。在去年横扫药物领域的医械临床实验核对大风暴中,也正是由于有知名大医院的涉嫌造假被查,而快速打破了药企纷纭观望的局面,主动撤回注册申请的药企数量短时间内大增。 固然,以总局首批抽查的这10家医疗器械企业的过往、范围等来看,被查出问题的可能性应当很小。 1切静待检查结果出炉! 医疗器械临床实验的核对会成为今年行业整理重点,这1点包括总局局长毕井泉亦曾公然表态。 而截至目前,除总局密集出台各种相干政策文件,包括《医疗器械临床实验质量管理规范》(以下简称《规范》)、医械临床实验检查要点等等,在地方,北京、山东、湖北、湖南这4个省分,已展开了医疗器械临床实验的自查核对。其中,湖北、湖南是在前不久才启动的。 另外,7月7日,浙江省药监局发布《浙江省食品药品监督管理局、浙江省卫生和计划生育委员会关于贯彻实行<医疗器械临床实验质量管理规范>的通知》(浙食药监规〔2016〕12号)和《医疗器械临床实验管理备案》办事流程文件。从2016年6月1日起,在浙江展开医疗器械临床实验的申办者、临床实验机构和研究者应严格依照《规范》要求展开临床实验。 浙江是第1个在CFDA发布《规范》以后,发出贯彻实行《规范》通知的省分。以后,应会有其他省分陆续跟进。 总局的抽查加上地方的自查、核对,和贯彻落实《规范》通知的出炉...未来几个月,医械临床实验数据真实性核对风暴,将席卷全国。
推荐阅读
-
 最红女星日版奶茶妹妹一缺陷被评在中国出不
最红女星日版奶茶妹妹一缺陷被评在中国出不不知道大家看过一部日本励志电影《垫底辣妹》吗?这部电影于2015年5月1日在日本上映,2016年4月14日在中国上映,...[详细]
-
 鹿晗关晓彤关系再升级两人同佩戴同款戒指
鹿晗关晓彤关系再升级两人同佩戴同款戒指鹿晗与关晓彤这对情侣自从公开恋情后经常被友扒出恩爱细节,不过近日鹿晗与关晓彤的关系疑从恋人再升级,两...[详细]
-
 明星街拍最美的刘雯樱花树下
明星街拍最美的刘雯樱花树下此页面是否是列表页或首页?未找到合适正文内容。种猪价格宝宝风寒感冒怎么办婴儿消化不良...[详细]
-
 谁能解释一下为什么石原里美顶一个油头也那
谁能解释一下为什么石原里美顶一个油头也那本文转载自OinFashion十元妹纸又出新电视剧——是一部以法医为题材的职场电视剧《UNNATURAL》又名《非自然死亡》电...[详细]
-
 女性向综艺盘点年龄段全幅化类型多样化垂直
女性向综艺盘点年龄段全幅化类型多样化垂直一线导读:女性群体成了观察的主题,而女性观众则成了锁定的目标,但在许多综艺中,女性仍然是 花瓶 角色,且...[详细]
-
 农农见老板范玮琪陈建州与陈立农合照笑容满
农农见老板范玮琪陈建州与陈立农合照笑容满陈立农范玮琪范玮琪、陈建州与陈立农四人合照 范范范瑋琪 嗨!@陈立农 农农~ 新浪娱乐讯 5月14日,范玮琪[微...[详细]
图文聚焦